Estérification
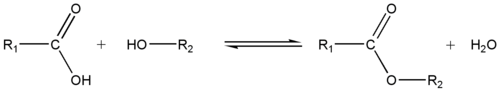
La réaction chimique qui produit un ester (+ H2O) à partir d'un alcool (R'-OH) et d'un acide carboxylique (R-COOH) est appelée estérification de Fisher. L'équation générale de cette réaction est :
- Note 1 : La réaction inverse est une hydrolyse.
- Note 2 : Cette réaction de synthèse est équilibrée lorsqu'elle est réalisée avec un acide (R-COOH), car la présence d'eau dans l'état final rend possible la réaction inverse, à savoir l'hydrolyse de l'ester. Cela limite donc le rendement de la réaction. Lorsque les réactifs sont utilisés dans les proportions stœchiométriques (1 pour 1), le rendement maximal est de 67% avec un alcool primaire (ex: ethanol), 60% avec un alcool secondaire (ex: isopropanol ou propan-2-ol) et 5% avec un alcool tertiaire (ex: tertbutanol ou 2-methylpropan-2-ol).Il est possible d'augmenter ces rendements par élimination d'eau au cours de la réaction (montage Dean-Starck).
L'utilisation de l'anhydride d'acide correspondant (R-COOCO-R) , en revanche, permet une réaction rapide et totale grâce à l'absence d'eau dans l'état final, selon l'équation :
Fichier:Réaction anhydride et alcool.png
Les chlorures d'acides (R-COCl) permettent d'obtenir le même résultat.
- Note 3 : par marquage isotopique, il a été démontré que l'oxygène présent dans l'eau formée provient de l'acide carboxylique
- Note 4 : les esters cycliques formés par réaction intramoléculaires sont appelés lactones
Les fonctions esters se retrouvent dans de nombreuses molécules biologiques, notamment les triglycérides. Plusieurs esters ont une odeur agréable et ils sont souvent à l'origine de l'arôme des fruits.