« Triméthylamine » : différence entre les versions
m Requête bot : Migration de {{Chimiebox}} |
m precAA=1 -> AA |
||
| Ligne 122 : | Ligne 122 : | ||
| 67548EEC = |
| 67548EEC = |
||
| 67548EECref = |
| 67548EECref = |
||
| symboles = | |
| symboles = |C|F+ |
||
| numeroIndex = {{indexCE|612-001-00-9}}<br />{{indexCE|612-001-01-6}} |
| numeroIndex = {{indexCE|612-001-00-9}}<br />{{indexCE|612-001-01-6}} |
||
| classificationCE = F+; R12 - Xn; R20/22 - C; R34 |
| classificationCE = F+; R12 - Xn; R20/22 - C; R34 |
||
| r = | |
| r = |R12|R34|R20/22 |
||
| s = <ref name="ESIS">{{ESIS|200-875-0|triméthylamine}}, consulté le 15 février 2009</ref>| |
| s = <ref name="ESIS">{{ESIS|200-875-0|triméthylamine}}, consulté le 15 février 2009</ref>|S1/2|S3|S16|S26|S29|S45|S36/37/39 |
||
| transportRef = |
| transportRef = |
||
| transport = {{ADR|Kemler=|ONU=1083|Classe=|CodeClassification=|Etiquette=|Etiquette2=|Etiquette3=|Emballage=}}<br /> |
| transport = {{ADR|Kemler=|ONU=1083|Classe=|CodeClassification=|Etiquette=|Etiquette2=|Etiquette3=|Emballage=}}<br /> |
||
Version du 6 février 2013 à 20:53
| Triméthylamine | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | N,N-dimethylmethanamine | |
| Synonymes |
Triméthylamine |
|
| No CAS | ||
| No ECHA | 100.000.796 | |
| No CE | 200-875-0 | |
| FEMA | 3241 | |
| Apparence | gaz comprimé liquefié incolore, d'odeur caractéristique. Ou solution incolore dans l'eau, d'odeur âcre. (solution aqueuse à 40 %)[1] |
|
| Propriétés chimiques | ||
| Formule | C3H9N [Isomères] |
|
| Masse molaire[3] | 59,110 3 ± 0,003 2 g/mol C 60,96 %, H 15,35 %, N 23,7 %, |
|
| pKa | 4,13 pKb | |
| Moment dipolaire | 0,612 ± 0,003 D [2] | |
| Propriétés physiques | ||
| T° fusion | −117 °C (pur)[1], −3 °C (solution à 40 %)[1] |
|
| T° ébullition | 3 °C (pur)[1], 30 °C (solution à 40 %)[1] |
|
| Solubilité | dans l'eau : très bonne | |
| Masse volumique | 0,6 g·cm-3 (liquide pur)[1], 0,9 g·cm-3 (solution à 40 %)[1] |
|
| T° d'auto-inflammation | 190 °C[1] | |
| Point d’éclair | −7 °C[1] | |
| Limites d’explosivité dans l’air | 2,0–11,6 %vol(pur)[1],2–16,6 %vol(solution à 40 %)[1] |
|
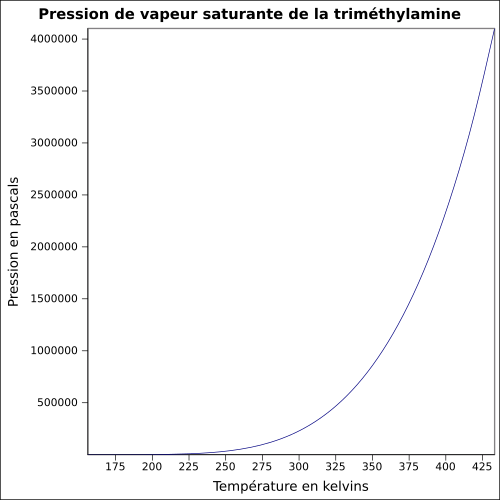
| Pression de vapeur saturante | 187 kPa (pur, 20 °C)[1], 67 kPa (solution à 40 %, 20 °C)[1] |
|
| Point critique | 40,9 bar, 160,15 °C [5] | |
| Thermochimie | ||
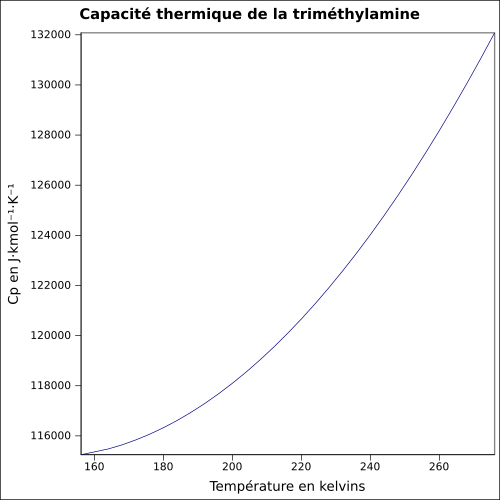
| Cp | ||
| Propriétés électroniques | ||
| 1re énergie d'ionisation | 7,82 ± 0,06 eV (gaz)[7] | |
| Précautions | ||
| SGH[9],[10] | ||
| H220, H315, H318, H332 et H335 H224, H302, H314 et H332 |
||
| SIMDUT[11] | ||
   A, B1, E, |
||
| NFPA 704 | ||
| Transport | ||
| Inhalation | Sensation de brûlure. Toux. Maux de tête. Mal de gorge. Respiration difficile. Essoufflement. Symptômes d'effets retardés | |
| Peau | Lors du contact avec le liquide : gelure. | |
| Yeux | Rougeur. Douleur. Troubles de la vue. | |
| Écotoxicologie | ||
| LogP | 0,2 (pur)[1], -0.3 (solution à 40 %)[1] |
|
| Seuil de l’odorat | bas : 0,000 11 ppm haut : 0,87 ppm[12] |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
La triméthylamine a pour formule C3H9N. Elle est dérivée de l'ammoniac dans lequel trois groupes –CH3 ont remplacé ses trois hydrogènes.
La triméthylamine est un gaz qui se liquéfie à 2 °C.
Elle dégage une odeur de poisson pourri sous l’action des enzymes et microbes sur les protéines de poisson. Elle est responsable de l’odeur des harengs marinés.
Utilisation
La triméthylamine est utilisée comme réactif intermédiaire dans la synthèse de nombreux produits organiques (produits pharmaceutiques, agriculture, colorants, caoutchoucs et produits explosifs ou propulseurs)[13].
En médecine
La triméthylaminurie est une maladie génétique, consistant en une concentration trop élevée en cette molécule dans les fluides corporels, secondaire à une mutation sur le gène codant pour une enzyme, la flavine-monooxygénase 3, permettant la dégradation de la molécule en un composé non odorant. La caractéristique principale de la maladie est l'odeur corporelle de poisson.
Notes et références
- TRIMETHYLAMINE et TRIMETHYLAMINE (solution aqueuse à 40 %), Fiches internationales de sécurité chimique
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 9-50
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 978-0-07-049841-9, LCCN 96051648), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 978-0-88415-857-8, LCCN 96036328)
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- « triméthylamine », sur ESIS, consulté le 15 février 2009
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Triméthylamine » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Trimethylamine », sur hazmap.nlm.nih.gov (consulté le )
- [1]