« Amine (chimie) » : différence entre les versions
Aucun résumé des modifications Balises : Suppression des portails Suppression de références Éditeur visuel |
Balises : Révocation manuelle Modification par mobile Modification par le web mobile |
||
| (41 versions intermédiaires par 29 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
{{Voir homonymes|Amine}} |
|||
[[Image:Ammonia.svg|thumb|right|100px|Ammoniac]] |
|||
[[Fichier:Ammonia.svg|vignette|100px|Structure de l'ammoniac.]] |
|||
Une '''amine''' est un [[composé organique]] dérivé de l'[[ammoniac]] dont au moins un [[atome d'hydrogène]] a été remplacé par un groupe carboné. Si l'un des atomes de carbone lié à l'atome d'[[azote]] (N) fait partie d'un [[Composé carbonylé|groupe carbonyle]], la molécule appartient à la famille des [[amide]]s. Découvertes en [[1849 en science|1849]] par [[Charles Adolphe Wurtz|Wurtz]], les amines furent initialement appelées « [[alcaloïde]]s artificiels ». |
|||
On parle d'amine primaire, secondaire ou tertiaire selon |
On parle d'amine [[primaire (chimie)|primaire]], [[secondaire (chimie)|secondaire]] ou [[tertiaire (chimie)|tertiaire]] selon qu'il y a un, deux ou trois radicaux (ou groupes) liés à l'atome d'azote. |
||
{| class="wikitable" style="margin: 1em auto 1em auto" |
{| class="wikitable" style="margin: 1em auto 1em auto" |
||
! Amine primaire || Amine secondaire || Amine tertiaire |
! Amine primaire || Amine secondaire || Amine tertiaire |
||
|- |
|- |
||
| |
| [[Fichier:Primary-amine-2D-general.png|100px|primary amine|center]] || [[Fichier:Secondary-amine-2D-general.png|100px|secondary amine|center]] || [[Fichier:Amine-2D-general.png|100px|tertiary amine|center]] |
||
|} |
|} |
||
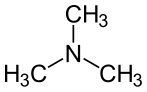
Par exemple, la [[triméthylamine]] est une amine tertiaire, de formule N(CH<sub>3</sub>)<sub>3</sub>. |
Par exemple, la [[triméthylamine]] est une amine tertiaire, de formule N(CH<sub>3</sub>)<sub>3</sub> car trois groupes [[méthyle]] sont liés à l'azote. |
||
[[ |
[[Fichier:Trimethylamin.svg|Triméthylamine]] |
||
== Nomenclature == |
== Nomenclature == |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
Sinon, elle possède le préfixe amino-. |
|||
| ⚫ | |||
== Synthèses == |
== Synthèses == |
||
Typiquement, les amines sont obtenues par [[alkylation]] d'amines de rang inférieur. |
Typiquement, les amines sont obtenues par [[alkylation]] d'amines de rang inférieur. En alkylant l'[[ammoniac]], on obtient des amines primaires, qui peuvent être alkylées en amines secondaires puis amines tertiaires. L'alkylation de ces dernières permet d'obtenir des sels d'[[ammonium quaternaire]]. |
||
En alkylant l'[[ammoniac]], on obtient des amines primaires, qui peuvent être alkylées en amines secondaires puis amines tertiaires. L'alkylation de ces dernières permet d'obtenir des sels d'[[ammonium quaternaire]]. |
|||
D'autre méthodes existent : |
D'autre méthodes existent : |
||
* |
* les amines primaires peuvent être obtenues par réduction d'un groupe [[azoture]] ; |
||
* |
* les amines peuvent aussi être obtenues par la [[Réaction d'oxydoréduction|réduction]] d'un [[amide]], à l'aide d'un [[hydrure]] ; |
||
* |
* l'[[amination réductrice]] permet l'obtention d'amines substituées à partir de [[composé carbonylé|composés carbonylés]] ([[aldéhyde]]s ou [[cétone]]s) ; |
||
* |
* les amines primaires peuvent être obtenues par la [[réaction de Gabriel]]. |
||
== Propriétés == |
== Propriétés == |
||
La présence de l'atome d'azote est la cause des propriétés des amines. |
La présence de l'atome d'azote est la cause des propriétés des amines. Cet atome présente un [[doublet non liant]], ce qui donne aux amines un caractère [[Base (chimie)|basique]] et [[nucléophile]]. |
||
| ⚫ | |||
Cet atome présente un [[doublet non liant]], ce qui donne aux amines un caractère basique et nucléophile. |
|||
| ⚫ | |||
Ils sont volatils, ont une odeur forte et sont hydrosolubles. |
|||
=== Dans le monde vivant === |
|||
== Types d'amines == |
|||
Les amines sont ubiquitairement présentes, en premier lieu avec les [[acides aminés]]. La dégradation des acides aminés est source de composés aminés perceptibles par l'odorat humain ; bien connues dans le cas des odeurs d'amines méthylées libérées par la putréfaction d'animaux, et notamment les crustacés ou poisson ([[triméthylamine]]). |
|||
| ⚫ | |||
Beaucoup de [[neurotransmetteur]]s sont des amines, dont l'[[épinéphrine]], la [[norépinéphrine]], la [[dopamine]], la [[sérotonine]] ou l'[[histamine]]. |
|||
| ⚫ | |||
Les groupes amine protonés ({{formule chimique|–NH|3|{{exp|+}}}}) sont les fractions de protéines les plus fréquemment chargés positivement, en particulier avec l'acide aminé [[lysine]]<ref>{{article|doi=10.1006/jmbi.1997.1498|titre=Adaptation of protein surfaces to subcellular location|année=1998|nom1=Andrade|prénom1=Miguel A.|nom2=O'Donoghue|prénom2=Seán I. |nom3=Rost |prénom3=Burkhard |journal=Journal of Molecular Biology|volume=276|numéro=2|pages=517–25|pmid=9512720|lire en ligne=https://www.rostlab.org/papers/1998_location/paper.pdf}}.</ref>. |
|||
| ⚫ | |||
L'[[ADN]] est un polymère anionique généralement lié à diverses protéines riches en amines<ref>{{Ouvrage|prénom1=D. L.|nom1=Nelson|prénom2=M. M.|nom2=Cox|titre=Lehninger, Principles of Biochemistry|lieu=New York|éditeur=Worth Publishing|année=2000|numéro d'édition=3|isbn=1-57259-153-6}}.</ref>. |
|||
En outre, l’ammonium primaire chargé en fin de chaîne sur la lysine peut former un pont avec des groupes [[carboxylate]] d’autres acides aminés dans certains [[polypeptide]]s ; c'est l’une des principales sources d'influences des structures tridimensionnelles des protéines<ref>{{article|doi=10.1021/bi00483a001|titre=Dominant forces in protein folding|année=1990|nom1=Dill|prénom1=Ken A. |journal=Biochemistry |volume=29 |numéro=31|pages=7133–55|pmid=2207096}}.</ref>. |
|||
== Typologie == |
|||
{{Article détaillé|Amine aromatique}} |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
== Les amines en milieu de travail (ressource externe) == |
== Les amines en milieu de travail (ressource externe) == |
||
| ⚫ | Les amines sont des composés organiques largement utilisés dans l’industrie et un récent rapport de recherche de l’[[Institut de recherche Robert-Sauvé en santé et en sécurité du travail]] (IRSST) a permis d’identifier les amines les plus susceptibles d’être retrouvées en milieu de travail québécois{{sfn|Ostiguy|Tranchand|Lesage|Van Tra|2003}}. |
||
| ⚫ | Les problèmes de santé pouvant se développer chez les travailleurs surexposés sont diversifiés, allant de l’[[Prurit|irritation cutanée]] au [[cancer]]. Les chercheurs de l'IRSST ont repéré un réactif qui permet de prélever simultanément trois amines différentes et d'en faire une analyse quantitative. Ils veulent poursuivre la mise au point de cette méthode analytique en utilisant le même réactif afin de recueillir et analyser une dizaine d'amines. Au terme de cette activité, l'IRSST disposera d'une méthode originale et validée d'échantillonnage et d'évaluation globale des amines, ce qui lui permettra de répondre aux demandes des intervenants en prévention. Cet outil permettra de mieux évaluer les risques de l'exposition professionnelle aux amines dans les entreprises{{sfn|Fournier|Ostiguy|Lesage|Van Tra|2007}}. |
||
== Références == |
|||
{{Références}} |
|||
== Voir aussi == |
|||
=== Articles connexes === |
|||
* [[Acide aminé]] |
|||
* [[Amine biogène]] |
|||
* [[Polyamine]] |
|||
* [[Nitrosation]] |
|||
* [[Nitrosamine]] |
|||
* [[Diamine]] |
|||
* [[Traitement des gaz par les amines]] |
|||
* [[Amines aliphatiques affections respiratoires (maladie professionnelle)]] |
|||
* [[Amines aromatiques allergies (maladie professionnelle)]] |
|||
* [[Test de Hinsberg]] |
|||
=== Bibliographie === |
|||
* {{Ouvrage|prénom1=C.|nom1=Ostiguy|prénom2=S.|nom2=Tranchand|prénom3=J.|nom3=Lesage|prénom4=H.|nom4=Van Tra|titre=Développement exploratoire d’une approche pour l’évaluation des amines en milieu de travail et documentation des procédés industriels utilisant ces substances|sous-titre=Rapport de recherche R-338|lieu=Montréal|éditeur=[[Institut de recherche Robert-Sauvé en santé et en sécurité du travail|IRSST]]|année=2003|isbn=|lire en ligne=http://www.irsst.qc.ca/fr/_publicationirsst_882.html}}. |
|||
* {{Ouvrage|prénom1=Mathieu|nom1=Fournier|prénom2=Claude|nom2=Ostiguy|prénom3=Jacques|nom3=Lesage|prénom4=Huu|nom4=Van Tra|titre=Méthode pour l'évaluation simultanée de différentes amines en milieu de travail|sous-titre=Rapport R-503|lieu=Montréal|éditeur=[[Institut de recherche Robert-Sauvé en santé et en sécurité du travail|IRSST]]|année=2007|isbn=|lire en ligne=http://www.irsst.qc.ca/fr/_publicationirsst_100295.html}}. |
|||
{{Portail|chimie}} |
|||
| ⚫ | Les amines sont des composés organiques largement utilisés dans l’industrie et un récent rapport de recherche de l’[[Institut de recherche Robert-Sauvé en santé et en sécurité du travail (IRSST) |
||
| ⚫ | |||
| ⚫ | |||
[[Catégorie:Groupe fonctionnel]] |
|||
| ⚫ | |||
Dernière version du 16 novembre 2023 à 14:21
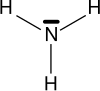
Une amine est un composé organique dérivé de l'ammoniac dont au moins un atome d'hydrogène a été remplacé par un groupe carboné. Si l'un des atomes de carbone lié à l'atome d'azote (N) fait partie d'un groupe carbonyle, la molécule appartient à la famille des amides. Découvertes en 1849 par Wurtz, les amines furent initialement appelées « alcaloïdes artificiels ».
On parle d'amine primaire, secondaire ou tertiaire selon qu'il y a un, deux ou trois radicaux (ou groupes) liés à l'atome d'azote.
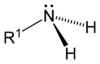
| Amine primaire | Amine secondaire | Amine tertiaire |
|---|---|---|
 |
 |
 |
Par exemple, la triméthylamine est une amine tertiaire, de formule N(CH3)3 car trois groupes méthyle sont liés à l'azote.
Nomenclature[modifier | modifier le code]
Si le groupe amine est prioritaire, la molécule comprend le suffixe « -amine ». Sinon, elle possède le préfixe « amino- ».
On les nomme comme des alcanamines substituées sur l'atome N : ainsi la triméthylamine (ancienne nomenclature) est la N,N-diméthylméthanamine (nom systématique IUPAC).
Synthèses[modifier | modifier le code]
Typiquement, les amines sont obtenues par alkylation d'amines de rang inférieur. En alkylant l'ammoniac, on obtient des amines primaires, qui peuvent être alkylées en amines secondaires puis amines tertiaires. L'alkylation de ces dernières permet d'obtenir des sels d'ammonium quaternaire.
D'autre méthodes existent :
- les amines primaires peuvent être obtenues par réduction d'un groupe azoture ;
- les amines peuvent aussi être obtenues par la réduction d'un amide, à l'aide d'un hydrure ;
- l'amination réductrice permet l'obtention d'amines substituées à partir de composés carbonylés (aldéhydes ou cétones) ;
- les amines primaires peuvent être obtenues par la réaction de Gabriel.
Propriétés[modifier | modifier le code]
La présence de l'atome d'azote est la cause des propriétés des amines. Cet atome présente un doublet non liant, ce qui donne aux amines un caractère basique et nucléophile. Dans le cas d'amines primaires et secondaires, la liaison N-H peut se rompre, ce qui leur donne un (faible) caractère acide, pour réagir avec des bases très fortes, comme les organomagnésiens.
Dans le monde vivant[modifier | modifier le code]
Les amines sont ubiquitairement présentes, en premier lieu avec les acides aminés. La dégradation des acides aminés est source de composés aminés perceptibles par l'odorat humain ; bien connues dans le cas des odeurs d'amines méthylées libérées par la putréfaction d'animaux, et notamment les crustacés ou poisson (triméthylamine).
Beaucoup de neurotransmetteurs sont des amines, dont l'épinéphrine, la norépinéphrine, la dopamine, la sérotonine ou l'histamine.
Les groupes amine protonés (–NH3+) sont les fractions de protéines les plus fréquemment chargés positivement, en particulier avec l'acide aminé lysine[1].
L'ADN est un polymère anionique généralement lié à diverses protéines riches en amines[2].
En outre, l’ammonium primaire chargé en fin de chaîne sur la lysine peut former un pont avec des groupes carboxylate d’autres acides aminés dans certains polypeptides ; c'est l’une des principales sources d'influences des structures tridimensionnelles des protéines[3].
Typologie[modifier | modifier le code]
En plus des amines primaires, secondaires ou tertiaires, on distingue les amines aliphatiques des amines aromatiques :
- les amines aromatiques présentent un ou plusieurs groupes phényle, qui rend difficile leur solubilité dans l'eau et dans le mucus nasal, ce groupe étant encombrant et apolaire ;
- les amines aliphatiques ont une structure linéaire ou ramifiée, et dégagent une odeur très forte. La cadavérine et la putrescine, par exemple, sont présentes dans la mauvaise haleine et dans l'urine.
Les amines en milieu de travail (ressource externe)[modifier | modifier le code]
Les amines sont des composés organiques largement utilisés dans l’industrie et un récent rapport de recherche de l’Institut de recherche Robert-Sauvé en santé et en sécurité du travail (IRSST) a permis d’identifier les amines les plus susceptibles d’être retrouvées en milieu de travail québécois[4].
Les problèmes de santé pouvant se développer chez les travailleurs surexposés sont diversifiés, allant de l’irritation cutanée au cancer. Les chercheurs de l'IRSST ont repéré un réactif qui permet de prélever simultanément trois amines différentes et d'en faire une analyse quantitative. Ils veulent poursuivre la mise au point de cette méthode analytique en utilisant le même réactif afin de recueillir et analyser une dizaine d'amines. Au terme de cette activité, l'IRSST disposera d'une méthode originale et validée d'échantillonnage et d'évaluation globale des amines, ce qui lui permettra de répondre aux demandes des intervenants en prévention. Cet outil permettra de mieux évaluer les risques de l'exposition professionnelle aux amines dans les entreprises[5].
Références[modifier | modifier le code]
- Miguel A. Andrade, Seán I. O'Donoghue et Burkhard Rost, « Adaptation of protein surfaces to subcellular location », Journal of Molecular Biology, vol. 276, no 2, , p. 517–25 (PMID 9512720, DOI 10.1006/jmbi.1997.1498, lire en ligne).
- D. L. Nelson et M. M. Cox, Lehninger, Principles of Biochemistry, New York, Worth Publishing, , 3e éd. (ISBN 1-57259-153-6).
- Ken A. Dill, « Dominant forces in protein folding », Biochemistry, vol. 29, no 31, , p. 7133–55 (PMID 2207096, DOI 10.1021/bi00483a001).
- Ostiguy et al. 2003.
- Fournier et al. 2007.
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Acide aminé
- Amine biogène
- Polyamine
- Nitrosation
- Nitrosamine
- Diamine
- Traitement des gaz par les amines
- Amines aliphatiques affections respiratoires (maladie professionnelle)
- Amines aromatiques allergies (maladie professionnelle)
- Test de Hinsberg
Bibliographie[modifier | modifier le code]
- C. Ostiguy, S. Tranchand, J. Lesage et H. Van Tra, Développement exploratoire d’une approche pour l’évaluation des amines en milieu de travail et documentation des procédés industriels utilisant ces substances : Rapport de recherche R-338, Montréal, IRSST, (lire en ligne).
- Mathieu Fournier, Claude Ostiguy, Jacques Lesage et Huu Van Tra, Méthode pour l'évaluation simultanée de différentes amines en milieu de travail : Rapport R-503, Montréal, IRSST, (lire en ligne).