« Catalyseur Phillips » : différence entre les versions
Catégorie:Synthèse des polymères, {{Palette|Matériaux polymères}} {{Portail|Chimie}} |
Fonctionnalité de suggestions de liens : 2 liens ajoutés. |
||
| (4 versions intermédiaires par 4 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
[[Fichier:PhillipsCatIdealized.svg|vignette|Structure proposée pour un catalyseur Phillips.]] |
[[Fichier:PhillipsCatIdealized.svg|vignette|Structure proposée pour un catalyseur Phillips.]] |
||
Le '''catalyseur Phillips''' ou catalyseur au chrome supporté de Phillips est un [[catalyseur]] utilisé pour produire environ la moitié du [[polyéthylène]] du monde<ref>{{ |
Le '''catalyseur Phillips''' ou catalyseur au chrome supporté de Phillips est un [[catalyseur]] utilisé pour produire environ la moitié du [[polyéthylène]] du monde<ref>{{article|journal = Catalysis Today|volume = 51|numéro = 2|date = 1999|pages = 215–221|doi = 10.1016/S0920-5861(99)00046-2|titre = Olefin polymerization over supported chromium oxide catalysts|prénom = Bert M.|nom = Weckhuysen|nom2 = Schoonheydt|prénom2 = Robert A.|url = http://dspace.library.uu.nl:8080/handle/1874/21357}}</ref>. [[Catalyseur hétérogène]], il est constitué d'un [[oxyde de chrome]] dispersé à la surface d’un support [[minéral]] de type [[Dioxyde de silicium|silice]] ou silice-[[alumine]] ([[zéolithe]])<ref>Max P. McDaniel "A Review of the Phillips Supported Chromium Catalyst and Its Commercial Use for Ethylene Polymerization" Advances in Catalysis, 2010, Volume 53, p. 123. {{Doi|10.1016/S0360-0564(10)53003-7}}</ref>. |
||
== |
== Historique == |
||
[[Robert Banks]] et [[John Paul Hogan]], tous deux chez Phillips Petroleum, ont déposé les premiers brevets sur ce catalyseur en 1953. Quatre ans plus tard, le procédé a été commercialisé<ref>J.P. Hogan, R.L. Banks, brevet américain 2,825,721 de Phillips Petroleum Company, rempli en août 1954 et publié en mars 1958.</ref>. |
[[Robert Banks]] et [[John Paul Hogan]], tous deux chez Phillips Petroleum, ont déposé les premiers brevets sur ce catalyseur en 1953. Quatre ans plus tard, le procédé a été commercialisé<ref>J.P. Hogan, R.L. Banks, brevet américain 2,825,721 de Phillips Petroleum Company, rempli en août 1954 et publié en mars 1958.</ref>. |
||
| Ligne 10 : | Ligne 10 : | ||
: n C<sub>2</sub>H<sub>4</sub> → (C<sub>2</sub>H<sub>4</sub>)<sub>n</sub> |
: n C<sub>2</sub>H<sub>4</sub> → (C<sub>2</sub>H<sub>4</sub>)<sub>n</sub> |
||
Bien qu'elle soit une [[réaction exergonique]] (c'est-à-dire thermodynamiquement favorable), la réaction de polymérisation de l'éthylène nécessite des catalyseurs. Trois catalyseurs principaux sont employés dans le commerce : les catalyseurs Phillips présentés ici, les catalyseurs [[Catalyse de Ziegler-Natta|de Ziegler-Natta]], et, pour les polymères de spécialité, les catalyseurs à base de [[métallocène]]. |
Bien qu'elle soit une [[réaction exergonique]] (c'est-à-dire thermodynamiquement favorable), la réaction de polymérisation de l'éthylène nécessite des catalyseurs. Trois catalyseurs principaux sont employés dans le commerce : les catalyseurs Phillips présentés ici, les catalyseurs [[Catalyse de Ziegler-Natta|de Ziegler-Natta]], et, pour les polymères de spécialité, les catalyseurs à base de [[métallocène]]<ref>Marc Carrega, « Aide-mémoire - Matières plastiques », {{Coll.|Aide-Mémoire}}, Dunod/''L'Usine nouvelle'', 2009, {{2e}}{{éd.}}, 256{{nb p.}}</ref>. |
||
== Préparation et mécanisme d'action == |
== Préparation et mécanisme d'action == |
||
Le catalyseur de Phillips est préparé en imprégnant du gel de silice à haute [[surface spécifique]] avec du [[trioxyde de chrome]] ou des composés de chrome apparentés. Ce pré-catalyseur solide est ensuite [[Calcination|calciné]] dans l'air pour donner le catalyseur actif. Seule une fraction du chrome est catalytiquement active, ce qui interfère avec l'élucidation du mécanisme catalytique. Le catalyseur actif est souvent décrit comme un [[ester]] de chromate lié à la surface de la silice. Le mécanisme du processus de polymérisation fait l'objet de nombreuses recherches, la question centrale étant la structure de l'espèce active, qui est supposée être un composé organochrome<ref>Klaus H. Theopold "Deprotonation of coordinated ethylene may start Phillips catalysis" Proceedings, U.S. National Academy of Sciences, 2014, vol. 111, pp. 11578-11579, {{Doi|10.1073/pnas.1411822111}}</ref>. |
Le catalyseur de Phillips est préparé en imprégnant du [[gel de silice]] à haute [[surface spécifique]] avec du [[trioxyde de chrome]] ou des composés de chrome apparentés. Ce pré-catalyseur solide est ensuite [[Calcination|calciné]] dans l'air pour donner le catalyseur actif. Seule une fraction du chrome est catalytiquement active, ce qui interfère avec l'élucidation du mécanisme catalytique. Le catalyseur actif est souvent décrit comme un [[ester]] de chromate lié à la surface de la silice. Le mécanisme du processus de polymérisation fait l'objet de nombreuses recherches, la question centrale étant la structure de l'espèce active, qui est supposée être un composé organochrome<ref>Klaus H. Theopold "Deprotonation of coordinated ethylene may start Phillips catalysis" Proceedings, U.S. National Academy of Sciences, 2014, vol. 111, pp. 11578-11579, {{Doi|10.1073/pnas.1411822111}}</ref>. |
||
== Références == |
== Références == |
||
Dernière version du 26 octobre 2023 à 23:34
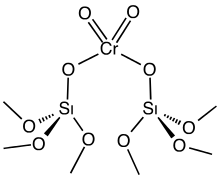
Le catalyseur Phillips ou catalyseur au chrome supporté de Phillips est un catalyseur utilisé pour produire environ la moitié du polyéthylène du monde[1]. Catalyseur hétérogène, il est constitué d'un oxyde de chrome dispersé à la surface d’un support minéral de type silice ou silice-alumine (zéolithe)[2].
Historique[modifier | modifier le code]
Robert Banks et John Paul Hogan, tous deux chez Phillips Petroleum, ont déposé les premiers brevets sur ce catalyseur en 1953. Quatre ans plus tard, le procédé a été commercialisé[3].
Contexte[modifier | modifier le code]
Le polyéthylène, polymère synthétique le plus abondant, est produit industriellement par polymérisation de l'éthylène :
- n C2H4 → (C2H4)n
Bien qu'elle soit une réaction exergonique (c'est-à-dire thermodynamiquement favorable), la réaction de polymérisation de l'éthylène nécessite des catalyseurs. Trois catalyseurs principaux sont employés dans le commerce : les catalyseurs Phillips présentés ici, les catalyseurs de Ziegler-Natta, et, pour les polymères de spécialité, les catalyseurs à base de métallocène[4].
Préparation et mécanisme d'action[modifier | modifier le code]
Le catalyseur de Phillips est préparé en imprégnant du gel de silice à haute surface spécifique avec du trioxyde de chrome ou des composés de chrome apparentés. Ce pré-catalyseur solide est ensuite calciné dans l'air pour donner le catalyseur actif. Seule une fraction du chrome est catalytiquement active, ce qui interfère avec l'élucidation du mécanisme catalytique. Le catalyseur actif est souvent décrit comme un ester de chromate lié à la surface de la silice. Le mécanisme du processus de polymérisation fait l'objet de nombreuses recherches, la question centrale étant la structure de l'espèce active, qui est supposée être un composé organochrome[5].
Références[modifier | modifier le code]
- Bert M. Weckhuysen et Robert A. Schoonheydt, « Olefin polymerization over supported chromium oxide catalysts », Catalysis Today, vol. 51, no 2, , p. 215–221 (DOI 10.1016/S0920-5861(99)00046-2, lire en ligne)
- Max P. McDaniel "A Review of the Phillips Supported Chromium Catalyst and Its Commercial Use for Ethylene Polymerization" Advances in Catalysis, 2010, Volume 53, p. 123. DOI 10.1016/S0360-0564(10)53003-7
- J.P. Hogan, R.L. Banks, brevet américain 2,825,721 de Phillips Petroleum Company, rempli en août 1954 et publié en mars 1958.
- Marc Carrega, « Aide-mémoire - Matières plastiques », coll. « Aide-Mémoire », Dunod/L'Usine nouvelle, 2009, 2e éd., 256 p.
- Klaus H. Theopold "Deprotonation of coordinated ethylene may start Phillips catalysis" Proceedings, U.S. National Academy of Sciences, 2014, vol. 111, pp. 11578-11579, DOI 10.1073/pnas.1411822111
