« Diamine » : différence entre les versions
m Retrait de 7 liens interlangues, désormais fournis par Wikidata sur la page d:q2500485 |
m →Diamines aromatiques : rectif lien image |
||
| (14 versions intermédiaires par 12 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
Une '''diamine''' est un type de [[polyamine]] contenant exactement deux groupes [[Amine (chimie)|amine]]. Les diamines sont principalement utilisées comme [[monomère]]s pour synthétiser des [[polyamide]]s, des [[polyimide]]s et des [[polyurée]]s. La principale diamine produite est le [[1,6-diaminohexane]], précurseur du [[Nylon 6-6]], suivie de l'[[éthylènediamine]]<ref |
Une '''diamine''' est un type de [[polyamine]] contenant exactement deux groupes [[Amine (chimie)|amine]]. Les diamines sont principalement utilisées comme [[monomère]]s pour synthétiser des [[polyamide]]s, des [[polyimide]]s et des [[polyurée]]s. La principale diamine produite est le [[1,6-diaminohexane]], précurseur du [[Nylon|nylon 6-6]], suivie de l'[[éthylènediamine]]<ref>Karsten Eller, Erhard Henkes, Roland Rossbacher et Hartmut Höke, ''Amines, Aliphatic'', dans ''[[Ullmann's Encyclopedia of Industrial Chemistry]]'', 2005, Wiley-VCH Verlag, Weinheim, {{doi|10.1002/14356007.a02_001}}.</ref>. L'[[hydrazine]] (H<sub>2</sub>NNH<sub>2</sub>) n'est en général pas considérée comme une diamine puisque ce n'est ni une amine (pas de carbone), ni une dibase. |
||
== Diamines aliphatiques == |
== Diamines aliphatiques == |
||
=== Diamines aliphatiques linéaires === |
=== Diamines aliphatiques linéaires === |
||
* 1 carbone : [[méthanediamine]]. |
|||
* 2 carbones: [[éthylènediamine]] (1,2-diaminoethane). Related derivatives include the N-alkylated compounds [[ethambutol]] and [[TMEDA]]. |
|||
* |
* 2 carbones : [[éthylènediamine]] (1,2-diaminoéthane). |
||
* |
* 3 carbones : [[1,3-diaminopropane]] (propane-1,3-diamine). |
||
* |
* 4 carbones : [[putrescine]] (butane-1,4-diamine). |
||
* |
* 5 carbones : [[cadavérine]] (pentane-1,5-diamine). |
||
* 6 carbones : [[hexaméthylènediamine]] (hexane-1,6-diamine). |
|||
<gallery> |
<gallery> |
||
Image:Ethylene_diamine.png|[[Éthylènediamine]] |
Image:Ethylene_diamine.png|[[Éthylènediamine]]. |
||
Image:1,3-Diaminopropane.svg|[[1,3- |
Image:1,3-Diaminopropane.svg|[[1,3-Diaminopropane]]. |
||
Image:Diaminobutane. |
Image:Diaminobutane.svg|[[Putrescine]]. |
||
Image: |
Image:Pentane-1,5-diamine 200.svg|[[Cadavérine]]. |
||
Image:1,6-diaminohexane-2D-skeletal.svg|[[Hexaméthylènediamine]] |
Image:1,6-diaminohexane-2D-skeletal.svg|[[Hexaméthylènediamine]]. |
||
</gallery> |
</gallery> |
||
=== Diamines aliphatiques ramifiées === |
=== Diamines aliphatiques ramifiées === |
||
On compte de nombreux dérivés de l'éthylènediamine: |
On compte de nombreux dérivés de l'éthylènediamine : |
||
* [[1,2-diaminopropane]] |
* [[1,2-diaminopropane]] ; |
||
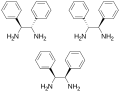
* [[diphényléthylènediamine]] |
* [[diphényléthylènediamine]] ; |
||
* [[1,2-diaminocyclohexane]] |
* [[1,2-diaminocyclohexane]]. |
||
<gallery> |
<gallery> |
||
Image: |
Image:Dpen_isomers.svg|[[Diphényléthylènediamine]]. |
||
Image:Trans-1,2-Diaminocyclohexane Structural Formulae V.1.svg|[[1,2- |
Image:Trans-1,2-Diaminocyclohexane Structural Formulae V.1.svg|[[1,2-Diaminocyclohexane]]. |
||
</gallery> |
</gallery> |
||
===Xylylènediamines=== |
=== Xylylènediamines === |
||
Les xylylènediamines sont classées parmi les alkylamines car les groupes amine ne sont pas directement attachés au cycle aromatique : |
Les xylylènediamines sont classées parmi les alkylamines car les groupes amine ne sont pas directement attachés au cycle aromatique : |
||
* o-xylylènediamine ou OXD |
* ''o''-xylylènediamine ou OXD ; |
||
* m-xylylènediamine ou MXD |
* ''m''-xylylènediamine ou MXD ; |
||
* p-xylylènediamine ou PXD |
* ''p''-xylylènediamine ou PXD. |
||
== Diamines aromatiques == |
== Diamines aromatiques == |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
<gallery> |
<gallery> |
||
Image:O-phenylenediamine.png| |
Image:O-phenylenediamine.png|[[o-Phénylènediamine|''o''-Phénylènediamine]]. |
||
Image:M-phenylenediamine.png| |
Image:M-phenylenediamine.png|[[m-Phénylènediamine|''m''-Phénylènediamine]]. |
||
Image:P-phenylenediamine. |
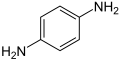
Image:P-phenylenediamine.svg|[[p-Phénylènediamine|''p''-Phénylènediamine]]. |
||
Image: |
Image:2,5-Diaminotoluol Structural Formula V1.svg|[[2,5-Diaminotoluène]]. |
||
</gallery> |
</gallery> |
||
Il existe de nombreux dérivés N-méthylés des |
Il existe de nombreux dérivés ''N''-méthylés des phénylènediamines : |
||
* [[diméthyl-4-phénylènediamine]], un réactif ; |
* [[diméthyl-4-phénylènediamine]], un réactif ; |
||
* [[N,N'-di-2-butyl-1,4-phénylènediamine]], un antioxydant. |
* [[N,N'-di-2-butyl-1,4-phénylènediamine|''N'',''N'''-di-2-butyl-1,4-phénylènediamine]], un [[antioxydant]]. |
||
<gallery> |
<gallery> |
||
Image:Dimethylphenylenediamine.png|[[Diméthyl-4-phénylènediamine]] |
Image:Dimethylphenylenediamine.png|[[Diméthyl-4-phénylènediamine]]. |
||
Image:N,N'- |
Image:N,N'-Di-sec-butyl-p-phenylendiamin.svg|[[N,N'-Di-2-butyl-1,4-phénylènediamine|''N'',''N'''-Di-2-butyl-1,4-phénylènediamine]]. |
||
</gallery> |
</gallery> |
||
Il existe aussi des diamines |
Il existe aussi des diamines aromatiques avec plusieurs cycles, par exemple des dérivés de [[biphényle]]s ou de [[naphtalène]]s : |
||
* [[benzidine|4,4'- |
* [[benzidine|4,4'-diaminobiphényle]] ; |
||
* [[1,8-diaminonaphtalène]] |
* [[1,8-diaminonaphtalène]]. |
||
<gallery> |
<gallery> |
||
Image:Benzidine structure.svg|[[benzidine|4,4'- |
Image:Benzidine structure.svg|[[benzidine|4,4'-Diaminobiphényle]]. |
||
Image:1,8-Diaminonaphthalene.png|[[1,8- |
Image:1,8-Diaminonaphthalene.png|[[1,8-Diaminonaphtalène]]. |
||
</gallery> |
</gallery> |
||
== Dérivés == |
== Dérivés == |
||
* [[Éthambutol]] |
* [[Éthambutol]] |
||
* [[EDTA]] (acide éthylènediaminetétraacétique) |
* [[EDTA]] (acide éthylènediaminetétraacétique) |
||
<gallery> |
<gallery> |
||
Image:Ethambutol.svg|[[Éthambutol]] |
Image:Ethambutol.svg|[[Éthambutol]]. |
||
Image: |
Image:EDTA.svg|[[EDTA]]. |
||
</gallery> |
</gallery> |
||
== Notes et références == |
== Notes et références == |
||
| ⚫ | |||
{{Références}} |
{{Références}} |
||
| ⚫ | |||
==Liens externes== |
== Liens externes == |
||
* {{MeshName|Diamines}} |
* {{MeshName|Diamines}} |
||
* {{en}} [ |
* {{en}} [https://www.organic-chemistry.org/synthesis/C1N/amines/diamines.shtm ''Synthesis of 1,2-diamines''], sur ''organic-chemistry.org'' |
||
{{Portail|Chimie}} |
{{Portail|Chimie}} |
||
[[Catégorie:Diamine| ]] |
[[Catégorie:Diamine| ]] |
||
[[Catégorie:Monomère]] |
|||
Dernière version du 27 août 2023 à 13:47
Une diamine est un type de polyamine contenant exactement deux groupes amine. Les diamines sont principalement utilisées comme monomères pour synthétiser des polyamides, des polyimides et des polyurées. La principale diamine produite est le 1,6-diaminohexane, précurseur du nylon 6-6, suivie de l'éthylènediamine[1]. L'hydrazine (H2NNH2) n'est en général pas considérée comme une diamine puisque ce n'est ni une amine (pas de carbone), ni une dibase.
Diamines aliphatiques[modifier | modifier le code]
Diamines aliphatiques linéaires[modifier | modifier le code]
- 1 carbone : méthanediamine.
- 2 carbones : éthylènediamine (1,2-diaminoéthane).
- 3 carbones : 1,3-diaminopropane (propane-1,3-diamine).
- 4 carbones : putrescine (butane-1,4-diamine).
- 5 carbones : cadavérine (pentane-1,5-diamine).
- 6 carbones : hexaméthylènediamine (hexane-1,6-diamine).
Diamines aliphatiques ramifiées[modifier | modifier le code]
On compte de nombreux dérivés de l'éthylènediamine :
Xylylènediamines[modifier | modifier le code]
Les xylylènediamines sont classées parmi les alkylamines car les groupes amine ne sont pas directement attachés au cycle aromatique :
- o-xylylènediamine ou OXD ;
- m-xylylènediamine ou MXD ;
- p-xylylènediamine ou PXD.
Diamines aromatiques[modifier | modifier le code]
Il existe trois phénylènediamines[2] :
- o-phénylènediamine ou OPD ;
- m-phénylènediamine ou MPD ;
- p-phénylènediamine ou PPD.
Le 2,5-diaminotoluène est proche de la PPD mais possède un groupe méthyle sur le cycle.
Il existe de nombreux dérivés N-méthylés des phénylènediamines :
- diméthyl-4-phénylènediamine, un réactif ;
- N,N'-di-2-butyl-1,4-phénylènediamine, un antioxydant.
Il existe aussi des diamines aromatiques avec plusieurs cycles, par exemple des dérivés de biphényles ou de naphtalènes :
Dérivés[modifier | modifier le code]
- Éthambutol
- EDTA (acide éthylènediaminetétraacétique)
-
EDTA.
Notes et références[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Diamine » (voir la liste des auteurs).
- Karsten Eller, Erhard Henkes, Roland Rossbacher et Hartmut Höke, Amines, Aliphatic, dans Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH Verlag, Weinheim, DOI 10.1002/14356007.a02_001.
- Robert A. Smiley, Phenylene- and Toluenediamines dans Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim, DOI 10.1002/14356007.a19_405.
Liens externes[modifier | modifier le code]
- (en) MeSH Diamines
- (en) Synthesis of 1,2-diamines, sur organic-chemistry.org