« Polytéréphtalate d'éthylène » : différence entre les versions
m LI |
m Suppression d'une phrase comportant un avis qui n'est pas nécessaire dans le propos. |
||
| (17 versions intermédiaires par 14 utilisateurs non affichées) | |||
| Ligne 167 : | Ligne 167 : | ||
[[File:Préforme PET avec bouchon.jpg|thumb|Préforme PET avec bouchon]] |
[[File:Préforme PET avec bouchon.jpg|thumb|Préforme PET avec bouchon]] |
||
Le '''poly(téréphtalate d'éthylène)'''<ref>Terminologie de la nomenclature officielle. Source : Marc Carrega, [[#Bibliographie|''op. cit.'']], {{p.|221, 224}}. Voir aussi la ''nomenclature'' dans l'article [[Polymère]].</ref>, plus connu sous le nom anglais de ''polyethylene terephthalate'' (parfois francisé de manière impropre en « |
Le '''poly(téréphtalate d'éthylène)'''<ref>Terminologie de la nomenclature officielle. Source : Marc Carrega, [[#Bibliographie|''op. cit.'']], {{p.|221, 224}}. Voir aussi la ''nomenclature'' dans l'article [[Polymère]].</ref>, plus connu sous le nom anglais de ''polyethylene terephthalate'' (parfois francisé de manière impropre en « polyéthylène téréphtalate ») ou '''PET''', que l'on trouve également avec l'abréviation '''PETE''', est un [[polymère]] de type [[polyester]] saturé [[thermoplastique]], par opposition aux polyesters [[thermodurcissable]]s. Ce [[polymère]] est obtenu par la [[Polymérisation par étapes|polycondensation]] de l'[[acide téréphtalique]] avec l'[[éthylène glycol]]. |
||
| ⚫ | Lors de la production du PET, les monomères sont condensés par [[estérification]] et la viscosité du matériau augmente progressivement jusqu'à obtenir à la fin de la polycondensation la consistance souhaitée. Ensuite, cette coulée chaude de {{tmp|250|°C}} est pressée à travers des buses en barres minces, puis refroidie et réduite en [[Granulé plastique|granulés]] qui seront par la suite mis en la forme désirée. |
||
| ⚫ | Le PET est un plastique pétrosourcé : les [[monomère]]s utilisés, l’éthylène glycol et l'acide téréphtalique, sont issus de la transformation du pétrole. Il faut {{unité|1.9|kg}} de [[pétrole brut]] pour fabriquer {{unité|1|kg}} de PET<ref>[http://www.strid.ch/Pdf/pet.pdf « |
||
| ⚫ | Refroidi brutalement, le PET est amorphe et transparent. Un refroidissement lent ou l'adjonction de germes de cristallisation ([[talc]], sulfate de baryum) peut le rendre translucide. Le [[taux de cristallinité]] ne dépasse cependant jamais 30 %, contre 60 % pour le [[Polytéréphtalate de butylène|poly(téréphtalate de butylène)]] (PBT)<ref name="trotignon">J.-P. Trotignon {{et al.}}, [[#Bibliographie|''op. cit.'']], {{p.|75}}.</ref>. |
||
| ⚫ | Lors de la production du PET, les monomères sont condensés par [[estérification]] et la viscosité du matériau augmente progressivement jusqu'à obtenir à la fin de la polycondensation la consistance souhaitée. Ensuite, cette coulée chaude de {{tmp|250|°C}} est pressée à travers des buses en barres minces, puis refroidie et réduite en [[Granulé plastique|granulés]]. |
||
| ⚫ | |||
| ⚫ | Refroidi brutalement, le PET est amorphe et transparent. Un refroidissement lent ou l'adjonction de germes de cristallisation (talc, sulfate de baryum) peut le rendre translucide. Le [[taux de cristallinité]] ne dépasse cependant jamais 30 %, contre 60 % pour le [[Polytéréphtalate de butylène|poly(téréphtalate de butylène)]] (PBT)<ref name="trotignon">J.-P. Trotignon {{et al.}}, [[#Bibliographie|''op. cit.'']], {{p.|75}}.</ref>. |
||
| ⚫ | |||
| ⚫ | Quant au PET des bouteilles d'[[eau gazeuse]] ou de limonade, (image ci-dessous à gauche de [[Moulage_par_injection_et_soufflage|l'injection et soufflage simple de telles bouteilles]]), il résiste à des pressions élevées de l’ordre de dix bars<ref>[https://en.calameo.com/books/000136672a94311404cc8 « Caractéristiques physico-chimiques des polymères et leurs températures de mise en forme - L'influence sur la température de fusion »], projet, sur [[Calaméo]].</ref> (d'où son utilisation pour la fabrication de [[fusée à eau|fusées à eau]] à une pression de lancement de cinq bars). |
||
Malgré sa dénomination, il n'y a aucune similitude avec le [[polyéthylène]] et il ne contient aucun [[phtalate]]<ref>{{Article|prénom = Patricia A.|nom = Enneking|titre = Phthalates Not in Plastic Food Packaging|périodique = Environmental Health Perspectives|volume = 114|date = 2006-02-01|issn = 0091-6765|pmid = 16451843|pmcid = 1367856|lire en ligne = https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1367856/|consulté le = 2016-02-17|pages = A89–A90}}</ref>. Des traces de [[Perturbateur endocrinien|perturbateurs endocriniens]] de type phtalate ou d'[[antimoine]] peuvent toutefois être retrouvées dans les produits alimentaires contenus dans des emballages en PET. Le dégagement de phtalate pourrait être dû aux sources utilisées dans le recyclage de PET et pourrait être plus élevé dans le cas des sodas et [[jus de fruits]] en raison de leur acidité. Quant à l'antimoine, il provient du [[catalyseur]] utilisé dans le processus de fabrication. Le dégagement d'antimoine de bouteilles en PET, trouvé dans {{nombre|132 marques}} de bouteilles d'eau provenant de {{nombre|28 pays}}, pourraient être lié à la température de conservation, comme dans le cas d'une bouteille restée dans une voiture exposée au soleil<ref name="Sax2010">{{Article|prénom = Leonard|nom = Sax|titre = Polyethylene Terephthalate May Yield Endocrine Disruptors|périodique = Environmental Health Perspectives|volume = 118|date = 2010-04-01|issn = 0091-6765|pmid = 20368129|pmcid = 2854718|doi = 10.1289/ehp.0901253|lire en ligne = https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2854718/|consulté le = 2016-02-17|pages = 445–448}}</ref>. Dans les deux cas, les autorités ont estimé que les niveaux atteints n'étaient pas alarmants. |
|||
| ⚫ | |||
| ⚫ | Le PET est un plastique pétrosourcé : les [[monomère]]s utilisés, l’éthylène glycol et l'acide téréphtalique, sont issus de la transformation du pétrole. Il faut {{unité|1.9|kg}} de [[pétrole brut]] pour fabriquer {{unité|1|kg}} de PET<ref>[http://www.strid.ch/Pdf/pet.pdf « PET »] {{pdf}}, sur ''strid.ch'', 2006.</ref>. |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | Quant au PET des bouteilles d'[[eau gazeuse]] ou de limonade, (image ci-dessous à gauche de [[Moulage_par_injection_et_soufflage|l'injection et soufflage simple de telles bouteilles]]), il résiste à des pressions élevées de l’ordre de dix bars<ref>[https://en.calameo.com/books/000136672a94311404cc8 « |
||
La molécule de poly(téréphtalate d'éthylène) s'hydrolyse à température élevée (environ {{tmp|240|°C}}), retournant vers une forme à bas poids moléculaire, inutilisable pour un usage habituel. Le polymère doit donc être soigneusement séché, sous vide à {{tmp|80|°C}}, avant utilisation<ref name="trotignon" />.<br /> C'est une limitation sévère à son [[Valorisation des déchets en matière plastique|recyclage]] économique comme matière réutilisable. |
La molécule de poly(téréphtalate d'éthylène) s'hydrolyse à température élevée (environ {{tmp|240|°C}}), retournant vers une forme à bas poids moléculaire, inutilisable pour un usage habituel. Le polymère doit donc être soigneusement séché, sous vide à {{tmp|80|°C}}, avant utilisation<ref name="trotignon" />.<br /> C'est une limitation sévère à son [[Valorisation des déchets en matière plastique|recyclage]] économique comme matière réutilisable. |
||
== Utilisations courantes == |
== Utilisations courantes == |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
* Rembourrage de peluches, de coussins. |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
* C'est l'un des matériaux utilisés par les [[Impression 3D|imprimantes 3D]], avec le [[nylon]] ou le [[Acide polylactique|PLA]]. |
|||
* en film (surface, 2D) : |
|||
== Utilisation spatiale == |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
** [[couverture de survie]] |
|||
| ⚫ | |||
| ⚫ | |||
** etc. |
|||
* en solide (3D) : |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
** [[Impression 3D]]. |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
** etc. |
|||
== Toxicité == |
== Toxicité == |
||
| ⚫ | |||
Comme l'ensemble des [[matière synthétique|matières synthétiques]], le PET subit les accusations classiques de toxicité, atteinte à la fertilité humaine (des [[fertilité masculine|hommes]] et des [[fertilité féminine|femmes]]){{etc.}} <ref>''Le Figaro.fr'', [http://www.lefigaro.fr/sante/2009/04/21/01004-20090421ARTFIG00013-faut-il-bannir-les-bouteilles-d-eau-en-plastique-.php ''Faut-il bannir les bouteilles d'eau en plastique ?''] {{Lien archive|url=http://www.lefigaro.fr/sante/2009/04/21/01004-20090421ARTFIG00013-faut-il-bannir-les-bouteilles-d-eau-en-plastique-.php |horodatage archive=20111015234233 |titre=Copie archivée}}, 21 avril 2009 (consulté le 11 janvier 2013).</ref>. Ces accusations sont étudiées par les autorités compétentes qui s'assurent que dans les conditions normales d'usage les risques sont absents<ref>[http://www.syndicat-ses.fr/upload/communique%20bfr%20all%20Internet.pdf ''Avis de l'Institut fédéral allemand d'évaluation des Risques (BfR)''] {{pdf}}</ref>{{,}}<ref>Jean-François Narbonne, [http://www.syndicat-ses.fr/upload/resume%20avis%20%20JFN%200204%2009.pdf « Résumé des commentaires sur la publication Wagner Oehlmann parue dans ''Environ. Sci. Pollut. Res.'' 2009 »] {{pdf}}</ref>. |
|||
=== Phtalates === |
|||
D'abord l'ensemble des phtalates a été suspecté, avec une présomption plus ou moins forte selon l'avancement des études<ref>Commission européenne, directive 92/32, annexe VI, 30 avril 1992</ref>, d'être toxique pour la reproduction, assez forte cependant pour que la Commission européenne ait programmé leur limitation<ref>Commission européenne, décision 815, 1999</ref> de plus en plus étendue<ref>Commission européenne, directive 84, 14 décembre 2005</ref>. |
|||
La toxicité présente ''a priori'' un risque pour les seuls [[Nouveau-né|bébés]], ceux-ci pouvant au cours d'opérations médicales recevoir jusqu'à plus de vingt fois la dose limite de {{unité|0.15|g}} de [[Phtalate de bis(2-éthylhexyle)|DEHP]] par jour pour un kilogramme de leur poids, ainsi que pour les [[adolescent]]s [[prépubère]]s en soins intensifs. C'est la façon dont le phtalate est associé au plastique qui fait que celui-ci peut migrer plus ou moins facilement dans l'organisme<ref>R. Causse et T. Sirdey, [https://ansm.sante.fr/var/ansm_site/storage/original/application/a71e772b5eccc88a7162758b5375e1bf.pdf ''Recommandations portant sur les phtalates dans les dispositifs médicaux''] {{pdf}}, Afssaps, département DEDIM, mars 2009.</ref>. Le risque n'est pas avéré avec le PET. Mais comme il est indiqué ci-dessus, le poly(téréphtalate d'éthylène) ne contient aucun phtalate, de sorte que les risques indiqués ne semblent pas s'appliquer. |
|||
Bien que son nom puisse l'associer aux [[phtalate]]s, le poly(téréphtalate d'éthylène) n'en contient normalement pas. Des traces ont pu être détectés sur du PET issu de recyclage, en raison du tri imparfait d'autres plastiques. |
|||
En 2007, la [[Suisse]] reconnait la toxicité du PET pour certains produits d'emballages. |
|||
Cette toxicité est due à l'un des composants du PET : l'[[antimoine]] (sous forme de traces provenant du [[catalyseur]] utilisé dans la réaction de [[polymérisation]] du PET) qui [[Contact alimentaire#Règlementation|migre du plastique aux denrées alimentaires]], plus facilement lorsqu'il est chauffé<ref>{{lien web|url=http://www.blv.admin.ch/themen/04678/04711/04713/index.html?lang=fr|titre=Analyse de risque - Antimoine dans les denrées alimentaires et repas de commodité conditionnés en barquettes de PET|site=blv.admin.ch|date=23 août 2007|consulté le=4 avril 2014}}.</ref>. L'antimoine (Sb) est un élément [[métalloïde]] utilisé comme catalyseur sous la forme de composés tels que le [[trioxyde d'antimoine]] ({{fchim|Sb|2|O|3}}) ou le [[triacétate d'antimoine]] dans la production de PET. Après la fabrication, une quantité détectable d'antimoine peut être trouvée à la surface du produit. Ce résidu peut être enlevé par lavage. L'antimoine restant dans le matériau lui-même peut aussi plus tard encore migrer vers les aliments et les boissons. |
|||
=== Antimoine === |
|||
L'antimoine (Sb) est un élément [[métalloïde]] utilisé comme catalyseur sous la forme de composés tels que le [[trioxyde d'antimoine]] ({{fchim|Sb|2|O|3}}) ou le [[triacétate d'antimoine]] dans la réaction de [[polymérisation]] pour la production de PET. Après la fabrication, une quantité détectable d'antimoine peut être trouvée à la surface du produit. Ce résidu peut être enlevé par lavage, mais l'antimoine restant dans le matériau lui-même peut aussi plus tard encore [[Contact alimentaire#Règlementation|migrer du plastique vers des denrées alimentaires]], plus facilement lorsqu'il est chauffé<ref>{{lien web|url=http://www.blv.admin.ch/themen/04678/04711/04713/index.html?lang=fr|titre=Analyse de risque - Antimoine dans les denrées alimentaires et repas de commodité conditionnés en barquettes de PET|site=blv.admin.ch|date=23 août 2007|consulté le=4 avril 2014}}.</ref>. |
|||
| ⚫ | L'OMS a publié une évaluation des risques liés à l'antimoine dans l'eau de boisson<ref name=GuideOMS/>. La limite maximale admissible d'antimoine pour l'eau potable a été fixée par l'OMS à vingt parties par milliard (OMS, 2003) et la limite pour l'[[eau potable]] aux États-Unis est quatre fois inférieure (de six parties par milliard)<ref>EPA (2003), ''Consumer Factsheet on: Antimony'', EPA archive, 2003-06-23</ref>. Bien que selon les recommandations de l'OMS pour les eaux de boissons, le [[trioxyde d'antimoine]] soit moins toxique lorsqu'il est pris par voie orale<ref name=GuideOMS>''Guidelines for drinking – water quality'', who.int</ref>, sa présence est prise en compte. |
||
L'exposition du PET à l'[[ébullition]] ou aux [[micro-onde]]s peut augmenter les niveaux d'antimoine de manière significative, éventuellement au-dessus des niveaux de contamination maximaux définis par l'[[Environmental Protection Agency|EPA]]<ref>Cheng X {{et al.}} (2010), ''Assessment of metal contaminations leaching out from recycling plastic bottles upon treatments'', ''Environmental science and pollution research international'', 17 (7), 1323–30, {{doi|10.1007/s11356-010-0312-4}}, {{PMID|20309737}}.</ref>. |
L'exposition du PET à l'[[ébullition]] ou aux [[micro-onde]]s peut augmenter les niveaux d'antimoine de manière significative, éventuellement au-dessus des niveaux de contamination maximaux définis par l'[[Environmental Protection Agency|EPA]]<ref>Cheng X {{et al.}} (2010), ''Assessment of metal contaminations leaching out from recycling plastic bottles upon treatments'', ''Environmental science and pollution research international'', 17 (7), 1323–30, {{doi|10.1007/s11356-010-0312-4}}, {{PMID|20309737}}.</ref>. |
||
| ⚫ | L’[[Office fédéral de la santé publique]] [[suisse]] a étudié l’importance de la migration de l’antimoine en comparant les eaux embouteillées en PET et en verre : les concentrations d’antimoine dans les bouteilles en PET étaient plus élevées, tout en restant nettement inférieures à la concentration maximale autorisée en Suisse. L’Office a conclu que de petites quantités d’antimoine migrant du PET vers de l’eau en bouteille, mais que le risque pour la santé des faibles concentrations en résultant est négligeable (1 % de la « dose journalière tolérable » telle que fixée par l’OMS). Trois ans plus tard, une autre étude (2006), plus largement médiatisée a confirmé des quantités similaires d'antimoine dans l'eau des bouteilles en PET au Canada et en Europe<ref>Shotyk William {{et al.}} (2006), ''Contamination of Canadian and European bottled waters with antimony from PET containers'', ''Journal of Environmental Monitoring'', 8 (2), 288–92, {{doi|10.1039/b517844b}}, {{PMID|16470261}}.</ref>. |
||
| ⚫ | La limite maximale admissible pour l'eau potable a été fixée par l'OMS à vingt parties par milliard (OMS, 2003) et la limite pour l'[[eau potable]] aux États-Unis est quatre fois inférieure (de six parties par milliard)<ref>EPA (2003), ''Consumer Factsheet on: Antimony'', EPA archive, 2003-06-23</ref>. Bien que selon les recommandations de l'OMS pour les eaux de boissons, le [[trioxyde d'antimoine]] soit moins toxique lorsqu'il est pris par voie orale<ref name=GuideOMS>''Guidelines for drinking – water quality'', who.int</ref>, sa présence |
||
| ⚫ | L’[[Office fédéral de la santé publique]] a étudié l’importance de la migration de l’antimoine en comparant les eaux embouteillées en PET et en verre : les concentrations d’antimoine dans les bouteilles en PET étaient plus élevées, tout en restant nettement inférieures à la concentration maximale autorisée en Suisse. L’Office a conclu que de petites quantités d’antimoine migrant du PET vers de l’eau en bouteille, mais que le risque pour la santé des faibles concentrations en résultant est négligeable (1 % de la « dose journalière tolérable » telle que fixée par l’OMS). Trois ans plus tard, une autre étude (2006), plus largement médiatisée a confirmé des quantités similaires d'antimoine dans l'eau des bouteilles en PET au Canada et en Europe<ref>Shotyk William {{et al.}} (2006), ''Contamination of Canadian and European bottled waters with antimony from PET containers'', ''Journal of Environmental Monitoring'', 8 (2), 288–92, {{doi|10.1039/b517844b}}, {{PMID|16470261}}.</ref>. |
||
L'OMS a publié une évaluation des risques liés à l'antimoine dans l'eau de boisson<ref name=GuideOMS/>. |
|||
En 2010, des concentrés de jus de fruits (pour lesquels aucune directive n'a été établie) produits et mis en bouteille en PET au [[Royaume-Uni]], contenaient jusqu'à {{unité|44,7 µg/L}} d'antimoine, bien au-dessus (près de neuf fois plus) que les limites fixées par l'UE pour l'eau du robinet de {{unité|5 µg/L}}, à titre de comparaison<ref>Hansen, Claus {{et al.}} (2010), ''Elevated antimony concentrations in commercial juices'', ''Journal of Environmental Monitoring'', 12 (4), 822–4, {{doi|10.1039/b926551a}}, {{PMID|20383361}}.</ref>{{,}}<ref>Borland, Sophie ({{1er}} mars 2010), ''Fruit juice cancer warning as scientists find harmful chemical in 16 drinks'', ''Daily Mail''.</ref>. |
En 2010, des concentrés de jus de fruits (pour lesquels aucune directive n'a été établie) produits et mis en bouteille en PET au [[Royaume-Uni]], contenaient jusqu'à {{unité|44,7 µg/L}} d'antimoine, bien au-dessus (près de neuf fois plus) que les limites fixées par l'UE pour l'eau du robinet de {{unité|5 µg/L}}, à titre de comparaison<ref>Hansen, Claus {{et al.}} (2010), ''Elevated antimony concentrations in commercial juices'', ''Journal of Environmental Monitoring'', 12 (4), 822–4, {{doi|10.1039/b926551a}}, {{PMID|20383361}}.</ref>{{,}}<ref>Borland, Sophie ({{1er}} mars 2010), ''Fruit juice cancer warning as scientists find harmful chemical in 16 drinks'', ''Daily Mail''.</ref>. |
||
== Biodégradation == |
== Biodégradation == |
||
| ⚫ | |||
Une espèce de [[bactérie]]s (classée dans le genre [[Nocardia]]) est connue comme pouvant [[biodégrader]] le PET, grâce à une [[enzyme]] ([[estérase]])<ref>{{Article |langue=en |nom1=Chetna |prénom1=Sharon |nom2=Madhuri |prénom2=Sharon |titre=''Studies on Biodegradation of Polyethylene terephthalate: A synthetic polymer'' |périodique=Journal of Microbiology and Biotechnology Research |volume=2 |numéro=2 |pages=248–257 |année=2012}}</ref>. |
Une espèce de [[bactérie]]s (classée dans le genre [[Nocardia]]) est connue comme pouvant [[biodégrader]] le PET, grâce à une [[enzyme]] ([[estérase]])<ref>{{Article |langue=en |nom1=Chetna |prénom1=Sharon |nom2=Madhuri |prénom2=Sharon |titre=''Studies on Biodegradation of Polyethylene terephthalate: A synthetic polymer'' |périodique=Journal of Microbiology and Biotechnology Research |volume=2 |numéro=2 |pages=248–257 |année=2012}}</ref>. |
||
Des chercheurs japonais ont isolé une [[bactérie]], ''[[Ideonella sakaiensis]]'', qui possède deux [[enzyme]]s capables de décomposer le PET en fragments plus petits, fragments que la bactérie peut ensuite digérer. Une colonie d'''I. sakaiensis'' peut désintégrer un fin film plastique de PET en six semaines environ<ref>{{Article |langue=en |auteur1=Yoshida, S. |auteur2=Hiraga, K. |auteur3=Takehana, T. |auteur4=Taniguchi, I. |auteur5=Yamaji, H. |auteur6=Maeda, Y. |auteur7=Toyohara, K. |auteur8=Miyamoto, K. |auteur9=Kimura, Y. |auteur10=Oda, K. |titre=''A bacterium that degrades and assimilates poly(ethylene terephthalate)'' |périodique=Science |volume=351 |numéro=6278 |pages=1196 |date=11 mars 2016 |doi=10.1126/science.aad6359 |pmid=26965627}}</ref>{{,}}<ref>{{Lien Web |langue=en |titre=''Could a new plastic-eating bacteria help combat this pollution scourge?'' |périodique=The Guardian |url=https://www.theguardian.com/environment/2016/mar/10/could-a-new-plastic-eating-bacteria-help-combat-this-pollution-scourge |date=10 mars 2016 |consulté le=23 mai 2020}}</ref>. |
Des chercheurs japonais ont isolé une [[bactérie]], ''[[Ideonella sakaiensis]]'', qui possède deux [[enzyme]]s capables de décomposer le PET en fragments plus petits, fragments que la bactérie peut ensuite digérer. Une colonie d'''I. sakaiensis'' peut désintégrer un fin film plastique de PET en six semaines environ<ref>{{Article |langue=en |auteur1=Yoshida, S. |auteur2=Hiraga, K. |auteur3=Takehana, T. |auteur4=Taniguchi, I. |auteur5=Yamaji, H. |auteur6=Maeda, Y. |auteur7=Toyohara, K. |auteur8=Miyamoto, K. |auteur9=Kimura, Y. |auteur10=Oda, K. |titre=''A bacterium that degrades and assimilates poly(ethylene terephthalate)'' |périodique=Science |volume=351 |numéro=6278 |pages=1196 |date=11 mars 2016 |doi=10.1126/science.aad6359 |pmid=26965627}}</ref>{{,}}<ref>{{Lien Web |langue=en |titre=''Could a new plastic-eating bacteria help combat this pollution scourge?'' |périodique=The Guardian |url=https://www.theguardian.com/environment/2016/mar/10/could-a-new-plastic-eating-bacteria-help-combat-this-pollution-scourge |date=10 mars 2016 |consulté le=23 mai 2020}}</ref>. |
||
En 2020, une autre enzyme, une [[cutinase]] nommée « LCC », initialement découverte par une équipe japonaise dans un compost de feuilles<ref>{{Article |langue=en |auteur1=Kitadokoro, K. |et al.=oui |titre=''Crystal structure of cutinase Est119 from Thermobifida alba AHK119 that can degrade modified polyethylene terephthalate at 1.76 Å resolution'' |périodique=Polymer Degradation and Stability |volume=97 |année=2012 |pages=771–775 |doi=10.1016/j.polymdegradstab.2012.02.003}}</ref>{{,}}<ref>{{Article |langue=en |auteur1=Sulaiman, S. |et al.=oui |titre=''Isolation of a novel cutinase homolog with polyethylene terephthalate-degrading activity from leaf-branch compost by using a metagenomics approach'' |périodique=Applied and Environmental Microbiology |volume=78 |année=2012 |pages=1556–1562 |doi=10.1128/AEM.06725-11}}</ref>, s'est révélée l'enzyme la plus efficace parmi toutes celles connues pour dépolymériser le PET, en étant capable de décomposer 90% de déchets de PET en 10 heures. Le PET est alors décomposé en ses deux monomères de base, le monoéthylène-glycol et l'acide téréphtalique, qui peut alors être réutilisé pour fabriquer de nouveaux objets en PET, équivalent à du PET en production primaire<ref>{{Article |langue=en |auteur1=Tournier, V. |auteur2=Topham, C.M. |auteur3=Gilles, A. |et al.=oui |titre=''An engineered PET depolymerase to break down and recycle plastic bottles'' |périodique=Nature |volume=580 |année=2020 |pages=216–219 |doi=10.1038/s41586-020-2149-4 |date=8 avril 2020 |consulté le=23 mai 2020}}</ref>. De manière naturelle, la cutinase « LCC » s'attaque à la cutine, un biopolymère lipidique intégré à la cuticule protégeant la surface des feuilles végétales, en coupant des liaisons ester. |
En 2020, une autre enzyme, une [[cutinase]] nommée « LCC », initialement découverte par une équipe japonaise dans un compost de feuilles<ref>{{Article |langue=en |auteur1=Kitadokoro, K. |et al.=oui |titre=''Crystal structure of cutinase Est119 from Thermobifida alba AHK119 that can degrade modified polyethylene terephthalate at 1.76 Å resolution'' |périodique=Polymer Degradation and Stability |volume=97 |année=2012 |pages=771–775 |doi=10.1016/j.polymdegradstab.2012.02.003}}</ref>{{,}}<ref>{{Article |langue=en |auteur1=Sulaiman, S. |et al.=oui |titre=''Isolation of a novel cutinase homolog with polyethylene terephthalate-degrading activity from leaf-branch compost by using a metagenomics approach'' |périodique=Applied and Environmental Microbiology |volume=78 |année=2012 |pages=1556–1562 |doi=10.1128/AEM.06725-11}}</ref>, s'est révélée l'enzyme la plus efficace parmi toutes celles connues pour dépolymériser le PET, en étant capable de décomposer 90% de déchets de PET en 10 heures. Le PET est alors décomposé en ses deux monomères de base, le [[Éthylène glycol|monoéthylène-glycol]] et l'[[acide téréphtalique]], qui peut alors être réutilisé pour fabriquer de nouveaux objets en PET, équivalent à du PET en production primaire<ref>{{Article |langue=en |auteur1=Tournier, V. |auteur2=Topham, C.M. |auteur3=Gilles, A. |et al.=oui |titre=''An engineered PET depolymerase to break down and recycle plastic bottles'' |périodique=Nature |volume=580 |année=2020 |pages=216–219 |doi=10.1038/s41586-020-2149-4 |date=8 avril 2020 |consulté le=23 mai 2020}}</ref>. De manière naturelle, la cutinase « LCC » s'attaque à la cutine, un biopolymère lipidique intégré à la cuticule protégeant la surface des feuilles végétales, en coupant des liaisons ester. |
||
== Commerce == |
== Commerce == |
||
[[File:Water Bottle Art.jpg|thumb|Bouteille PET commercialisée avec le [[Cervin]] en relief]] |
|||
En 2014, la France était nette importatrice de PET, avec une moyenne d'import mensuelle de {{unité|27000|t}}, contre des exportations s'élevant à {{unité|1800|t}}. La même année, le prix moyen du PET construit à partir des données des douanes françaises était de {{unité|1100|€/t}}<ref>{{Lien web|titre = Indicateur des échanges import/export |url =http://lekiosque.finances.gouv.fr/LEO/frame_LEO.asp|site =Direction générale des douanes. Indiquer NC8=39076020 |consulté le = 7 août 2015}}</ref>. |
En 2014, la France était nette importatrice de PET, avec une moyenne d'import mensuelle de {{unité|27000|t}}, contre des exportations s'élevant à {{unité|1800|t}}. La même année, le prix moyen du PET construit à partir des données des douanes françaises était de {{unité|1100|€/t}}<ref>{{Lien web|titre = Indicateur des échanges import/export |url =http://lekiosque.finances.gouv.fr/LEO/frame_LEO.asp|site =Direction générale des douanes. Indiquer NC8=39076020 |consulté le = 7 août 2015}}</ref>. |
||
Version du 24 août 2023 à 15:09
| Poly(téréphtalate d'éthylène) | |
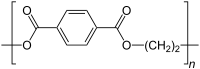
| |
| Structure du poly(téréphtalate d'éthylène) -[O-(CH2)2-O-CO-pPh-CO]n- |
|
| Identification | |
|---|---|
| Nom UICPA | poly(oxyéthylène oxytéréphtaloyle) |
| Synonymes |
PET |
| No CAS | |
| No ECHA | 100.121.858 |
| SMILES | |
| Propriétés chimiques | |
| Formule | (C10H8O4)n |
| Propriétés physiques | |
| T° transition vitreuse | 70 °C[1] |
| T° fusion | 245 °C |
| Paramètre de solubilité δ | 20,5 J1/2 cm−3/2[2] ; 21,9 MPa1/2[3] |
| Masse volumique | 1,34–1,39 g cm−3[4] |
| Conductivité thermique | 0,15 W m−1 K−1[4] |
| Propriétés électroniques | |
| Constante diélectrique | 3,25 (1 kHz, 23 °C) 3 (1 MHz, 23 °C) 2,8 (1 GHz, 23 °C)[5] |
| Propriétés optiques | |
| Indice de réfraction | 1,57–1,58[4] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|


Le poly(téréphtalate d'éthylène)[6], plus connu sous le nom anglais de polyethylene terephthalate (parfois francisé de manière impropre en « polyéthylène téréphtalate ») ou PET, que l'on trouve également avec l'abréviation PETE, est un polymère de type polyester saturé thermoplastique, par opposition aux polyesters thermodurcissables. Ce polymère est obtenu par la polycondensation de l'acide téréphtalique avec l'éthylène glycol.
Lors de la production du PET, les monomères sont condensés par estérification et la viscosité du matériau augmente progressivement jusqu'à obtenir à la fin de la polycondensation la consistance souhaitée. Ensuite, cette coulée chaude de 250 °C est pressée à travers des buses en barres minces, puis refroidie et réduite en granulés qui seront par la suite mis en la forme désirée.
Refroidi brutalement, le PET est amorphe et transparent. Un refroidissement lent ou l'adjonction de germes de cristallisation (talc, sulfate de baryum) peut le rendre translucide. Le taux de cristallinité ne dépasse cependant jamais 30 %, contre 60 % pour le poly(téréphtalate de butylène) (PBT)[7].
Par extrusion et étirage sous tension, on obtient à partir du PET amorphe un film aux propriétés biaxiales semi-cristallines. Ce film de très grande solidité en tension, très stable et transparent, très bon isolant électrique, est connu sous les marques Mylar, Melinex et Hostaphan.
Quant au PET des bouteilles d'eau gazeuse ou de limonade, (image ci-dessous à gauche de l'injection et soufflage simple de telles bouteilles), il résiste à des pressions élevées de l’ordre de dix bars[8] (d'où son utilisation pour la fabrication de fusées à eau à une pression de lancement de cinq bars).
Malgré sa dénomination, il n'y a aucune similitude avec le polyéthylène et il ne contient aucun phtalate[9]. Des traces de perturbateurs endocriniens de type phtalate ou d'antimoine peuvent toutefois être retrouvées dans les produits alimentaires contenus dans des emballages en PET. Le dégagement de phtalate pourrait être dû aux sources utilisées dans le recyclage de PET et pourrait être plus élevé dans le cas des sodas et jus de fruits en raison de leur acidité. Quant à l'antimoine, il provient du catalyseur utilisé dans le processus de fabrication. Le dégagement d'antimoine de bouteilles en PET, trouvé dans 132 marques de bouteilles d'eau provenant de 28 pays, pourraient être lié à la température de conservation, comme dans le cas d'une bouteille restée dans une voiture exposée au soleil[10]. Dans les deux cas, les autorités ont estimé que les niveaux atteints n'étaient pas alarmants.
Le PET est un plastique pétrosourcé : les monomères utilisés, l’éthylène glycol et l'acide téréphtalique, sont issus de la transformation du pétrole. Il faut 1,9 kg de pétrole brut pour fabriquer 1 kg de PET[11].
La molécule de poly(téréphtalate d'éthylène) s'hydrolyse à température élevée (environ 240 °C), retournant vers une forme à bas poids moléculaire, inutilisable pour un usage habituel. Le polymère doit donc être soigneusement séché, sous vide à 80 °C, avant utilisation[7].
C'est une limitation sévère à son recyclage économique comme matière réutilisable.
Utilisations courantes

- en fil : innombrables usages en Fibre textile (y compris « polaires » ou « microfibre ») pour la confection de vêtements (notamment à base de PET recyclé), le rembourrage de peluches, coussins, couettes, vêtements, etc.
- en film (surface, 2D) :
- Revêtement intérieur de canettes et conserves, aluminium ou acier, pour éviter le contact avec les aliments.
- Chemisage des canalisations en plomb.
- Films transparents à bas coût pour les applications d'optique (écrans LCD, instruments).
- La voile des deltaplanes très performants.
- Un prototype de voile solaire (LightSail-1) a été déployé avec succès en orbite basse en . Ce démonstrateur technologique comportait une voile solaire d'une superficie de 32 m2 (5,6 × 5,6 m) réalisée en Mylar.
- Sans danger pour le papier, il est utilisé dans le cadre du projet de préservation des comics.
- Sur des peaux de batterie, sous forme d'un film fin, disposé afin d'augmenter la solidité et la résistance de la peau.
- couverture de survie
- Emballages résistant au four.
- Protection de plateaux de jeux pour flipper.
- etc.
- en solide (3D) :
- Bon nombre de cartes de format « carte de crédit » type carte de membre, fidélité, réduction, client, etc. Elles peuvent être aussi en PVC ou en PC (polycarbonate).
- Bouteilles recyclables, le PET est étanche au CO2, d'où son utilisation pour les bouteilles de limonade et autres boissons effervescentes (animation ci-dessus).
- Emballages jetables de toutes sortes (boîtes pour les salades, plateaux de présentation, etc.).
- Impression 3D.
- Métallisé, lunettes d'observation des éclipses solaires.
- Plaques imprimées puis thermoformées pour la fabrication d'enseignes lumineuses.
- Plumes pour flèches de compétition.
- Plastie ligamentaire et chirurgie reconstructrice.
- Prothèses cardio-vasculaires.
- etc.
Toxicité
Comme l'ensemble des matières synthétiques, le PET subit les accusations classiques de toxicité, atteinte à la fertilité humaine (des hommes et des femmes), etc. [12]. Ces accusations sont étudiées par les autorités compétentes qui s'assurent que dans les conditions normales d'usage les risques sont absents[13],[14].
Phtalates
Bien que son nom puisse l'associer aux phtalates, le poly(téréphtalate d'éthylène) n'en contient normalement pas. Des traces ont pu être détectés sur du PET issu de recyclage, en raison du tri imparfait d'autres plastiques.
Antimoine
L'antimoine (Sb) est un élément métalloïde utilisé comme catalyseur sous la forme de composés tels que le trioxyde d'antimoine (Sb2O3) ou le triacétate d'antimoine dans la réaction de polymérisation pour la production de PET. Après la fabrication, une quantité détectable d'antimoine peut être trouvée à la surface du produit. Ce résidu peut être enlevé par lavage, mais l'antimoine restant dans le matériau lui-même peut aussi plus tard encore migrer du plastique vers des denrées alimentaires, plus facilement lorsqu'il est chauffé[15].
L'OMS a publié une évaluation des risques liés à l'antimoine dans l'eau de boisson[16]. La limite maximale admissible d'antimoine pour l'eau potable a été fixée par l'OMS à vingt parties par milliard (OMS, 2003) et la limite pour l'eau potable aux États-Unis est quatre fois inférieure (de six parties par milliard)[17]. Bien que selon les recommandations de l'OMS pour les eaux de boissons, le trioxyde d'antimoine soit moins toxique lorsqu'il est pris par voie orale[16], sa présence est prise en compte.
L'exposition du PET à l'ébullition ou aux micro-ondes peut augmenter les niveaux d'antimoine de manière significative, éventuellement au-dessus des niveaux de contamination maximaux définis par l'EPA[18].
L’Office fédéral de la santé publique suisse a étudié l’importance de la migration de l’antimoine en comparant les eaux embouteillées en PET et en verre : les concentrations d’antimoine dans les bouteilles en PET étaient plus élevées, tout en restant nettement inférieures à la concentration maximale autorisée en Suisse. L’Office a conclu que de petites quantités d’antimoine migrant du PET vers de l’eau en bouteille, mais que le risque pour la santé des faibles concentrations en résultant est négligeable (1 % de la « dose journalière tolérable » telle que fixée par l’OMS). Trois ans plus tard, une autre étude (2006), plus largement médiatisée a confirmé des quantités similaires d'antimoine dans l'eau des bouteilles en PET au Canada et en Europe[19].
En 2010, des concentrés de jus de fruits (pour lesquels aucune directive n'a été établie) produits et mis en bouteille en PET au Royaume-Uni, contenaient jusqu'à 44,7 µg/L d'antimoine, bien au-dessus (près de neuf fois plus) que les limites fixées par l'UE pour l'eau du robinet de 5 µg/L, à titre de comparaison[20],[21].
Biodégradation

Une espèce de bactéries (classée dans le genre Nocardia) est connue comme pouvant biodégrader le PET, grâce à une enzyme (estérase)[22].
Des chercheurs japonais ont isolé une bactérie, Ideonella sakaiensis, qui possède deux enzymes capables de décomposer le PET en fragments plus petits, fragments que la bactérie peut ensuite digérer. Une colonie d'I. sakaiensis peut désintégrer un fin film plastique de PET en six semaines environ[23],[24].
En 2020, une autre enzyme, une cutinase nommée « LCC », initialement découverte par une équipe japonaise dans un compost de feuilles[25],[26], s'est révélée l'enzyme la plus efficace parmi toutes celles connues pour dépolymériser le PET, en étant capable de décomposer 90% de déchets de PET en 10 heures. Le PET est alors décomposé en ses deux monomères de base, le monoéthylène-glycol et l'acide téréphtalique, qui peut alors être réutilisé pour fabriquer de nouveaux objets en PET, équivalent à du PET en production primaire[27]. De manière naturelle, la cutinase « LCC » s'attaque à la cutine, un biopolymère lipidique intégré à la cuticule protégeant la surface des feuilles végétales, en coupant des liaisons ester.
Commerce

En 2014, la France était nette importatrice de PET, avec une moyenne d'import mensuelle de 27 000 t, contre des exportations s'élevant à 1 800 t. La même année, le prix moyen du PET construit à partir des données des douanes françaises était de 1 100 €/t[28].
En 2003, dans les commerces suisses, huit bouteilles sur dix étaient en PET[29]. En 2011, cela représente 1,2 milliard de bouteilles en PET mises sur le marché[réf. nécessaire].
Recyclage
La Suisse est leader mondial en matière de recyclage des bouteilles en PET. En 2010, plus de 80 % d'entre elles retournent à la fabrique après usage[29], contre 94 % pour le verre et 91 % pour les canettes en aluminium[30], ce qui représente 700 millions de bouteilles récupérées par an[29].
Notes et références
- (en) Charles E. Wilkes, James W. Summers, Charles Anthony Daniels et Mark T. Berard, PVC Handbook, Munich, Hanser Verlag, , 1re éd., 723 p. (ISBN 978-1-56990-379-7, LCCN 2005013540, lire en ligne)
- (en) Yves Gnanou et Michel Fontanille, Organic and Physical Chemistry of Polymers, Hoboken (N.J.), John Wiley & Sons, , 617 p. (ISBN 978-0-471-72543-5), p. 17
- (en) Leslie Howard Sperling, Introduction to Physical Polymer Science, Hoboken, New Jersey, Wiley, , 845 p. (ISBN 978-0-471-70606-9, lire en ligne), p. 75
- (en) J. G. Speight et Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.807 et 2.758
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press, , 90e éd., 2804 p., relié (ISBN 978-1-4200-9084-0)
- Terminologie de la nomenclature officielle. Source : Marc Carrega, op. cit., p. 221, 224. Voir aussi la nomenclature dans l'article Polymère.
- J.-P. Trotignon et al., op. cit., p. 75.
- « Caractéristiques physico-chimiques des polymères et leurs températures de mise en forme - L'influence sur la température de fusion », projet, sur Calaméo.
- Patricia A. Enneking, « Phthalates Not in Plastic Food Packaging », Environmental Health Perspectives, vol. 114, , A89–A90 (ISSN 0091-6765, PMID 16451843, PMCID 1367856, lire en ligne, consulté le )
- Leonard Sax, « Polyethylene Terephthalate May Yield Endocrine Disruptors », Environmental Health Perspectives, vol. 118, , p. 445–448 (ISSN 0091-6765, PMID 20368129, PMCID 2854718, DOI 10.1289/ehp.0901253, lire en ligne, consulté le )
- « PET » [PDF], sur strid.ch, 2006.
- Le Figaro.fr, Faut-il bannir les bouteilles d'eau en plastique ? « Copie archivée » (version du sur Internet Archive), 21 avril 2009 (consulté le 11 janvier 2013).
- Avis de l'Institut fédéral allemand d'évaluation des Risques (BfR) [PDF]
- Jean-François Narbonne, « Résumé des commentaires sur la publication Wagner Oehlmann parue dans Environ. Sci. Pollut. Res. 2009 » [PDF]
- « Analyse de risque - Antimoine dans les denrées alimentaires et repas de commodité conditionnés en barquettes de PET », sur blv.admin.ch, (consulté le ).
- Guidelines for drinking – water quality, who.int
- EPA (2003), Consumer Factsheet on: Antimony, EPA archive, 2003-06-23
- Cheng X et al. (2010), Assessment of metal contaminations leaching out from recycling plastic bottles upon treatments, Environmental science and pollution research international, 17 (7), 1323–30, DOI 10.1007/s11356-010-0312-4, .
- Shotyk William et al. (2006), Contamination of Canadian and European bottled waters with antimony from PET containers, Journal of Environmental Monitoring, 8 (2), 288–92, DOI 10.1039/b517844b, .
- Hansen, Claus et al. (2010), Elevated antimony concentrations in commercial juices, Journal of Environmental Monitoring, 12 (4), 822–4, DOI 10.1039/b926551a, .
- Borland, Sophie (1er mars 2010), Fruit juice cancer warning as scientists find harmful chemical in 16 drinks, Daily Mail.
- (en) Sharon Chetna et Sharon Madhuri, « Studies on Biodegradation of Polyethylene terephthalate: A synthetic polymer », Journal of Microbiology and Biotechnology Research, vol. 2, no 2, , p. 248–257
- (en) Yoshida, S., Hiraga, K., Takehana, T., Taniguchi, I., Yamaji, H., Maeda, Y., Toyohara, K., Miyamoto, K., Kimura, Y. et Oda, K., « A bacterium that degrades and assimilates poly(ethylene terephthalate) », Science, vol. 351, no 6278, , p. 1196 (PMID 26965627, DOI 10.1126/science.aad6359)
- (en) « Could a new plastic-eating bacteria help combat this pollution scourge? », The Guardian, (consulté le )
- (en) Kitadokoro, K. et al., « Crystal structure of cutinase Est119 from Thermobifida alba AHK119 that can degrade modified polyethylene terephthalate at 1.76 Å resolution », Polymer Degradation and Stability, vol. 97, , p. 771–775 (DOI 10.1016/j.polymdegradstab.2012.02.003)
- (en) Sulaiman, S. et al., « Isolation of a novel cutinase homolog with polyethylene terephthalate-degrading activity from leaf-branch compost by using a metagenomics approach », Applied and Environmental Microbiology, vol. 78, , p. 1556–1562 (DOI 10.1128/AEM.06725-11)
- (en) Tournier, V., Topham, C.M., Gilles, A. et al., « An engineered PET depolymerase to break down and recycle plastic bottles », Nature, vol. 580, , p. 216–219 (DOI 10.1038/s41586-020-2149-4)
- « Indicateur des échanges import/export », sur Direction générale des douanes. Indiquer NC8=39076020 (consulté le )
- « Le recyclage de PET, une spécialité suisse », Swissinfo, (consulté le )
- « Les Suisses, as du recyclage du PET et du verre », RTS Info, (consulté le )
Voir aussi
Articles connexes
Bibliographie
- Marc Carrega, Les Polymères : de la molécule à l'objet, Les Ulis (France, EDP sciences, coll. « Monographie de matérialogie » (no 4), , 233 p. (ISBN 978-2-86883-390-7 et 2-868-83390-X, BNF 37043142)
- J.-P. Trotignon et al., Précis de Matières plastiques, Structure-Propriétés, Mise en œuvre, Normalisation AFNOR, Nathan, 1996, Nathan (ISBN 2091765724), AFNOR (ISBN 2124250213)

